1. 行业背景与MaXFlow的破局之道
MaXFlow 逆向AI实验设计智能体加速CMC工艺与配方设计优化
在现代创新药的CMC阶段,无论是小分子药物的合成工艺,还是大分子生物制剂的配方开发,都面临着“设计空间庞大”与“实验资源有限”的核心矛盾 。传统的实验设计(DOE,如 Central Composite Design 或 Box-Behnken Design)在处理高阶复杂性时往往捉襟见肘,极易陷入局部最优,且对实验量的需求极大 。
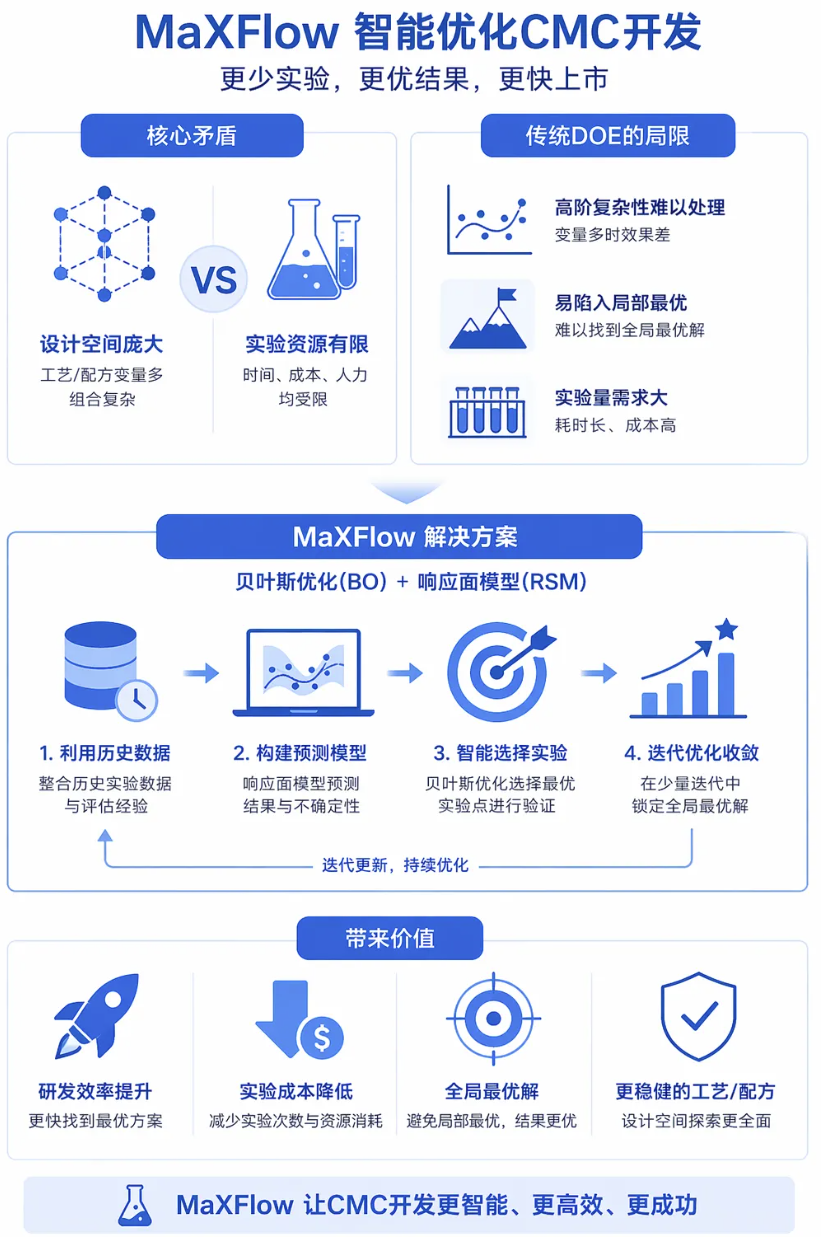
MaXFlow平台通过引入先进的贝叶斯优化(Bayesian Optimization, BO)算法与响应面模型相结合,彻底颠覆了传统的单因素与正交设计模式 。它能够利用历史数据和评估经验来智能指导未来的实验选择,在极少的迭代次数内锁定全局最优解,显著提升研发效率并降低成本 。
2. 核心应用场景一:小分子药物合成工艺优化
MaXFlow 逆向AI实验设计智能体加速CMC工艺与配方设计优化
在小分子合成中,关键催化反应的条件筛选往往决定了最终的产率与成本。
2.1 痛点:庞大的反应空间与低反应性
以 JAK2 抑制剂 BMS-911543 商业化合成中的关键步骤——钯催化咪唑直接芳基化反应为例 。该反应属于钯催化 C-H 官能团化反应,其核心挑战在于杂环底物反应性极低,需要精准调控配体、碱、溶剂等参数以提升产率与选择性 。
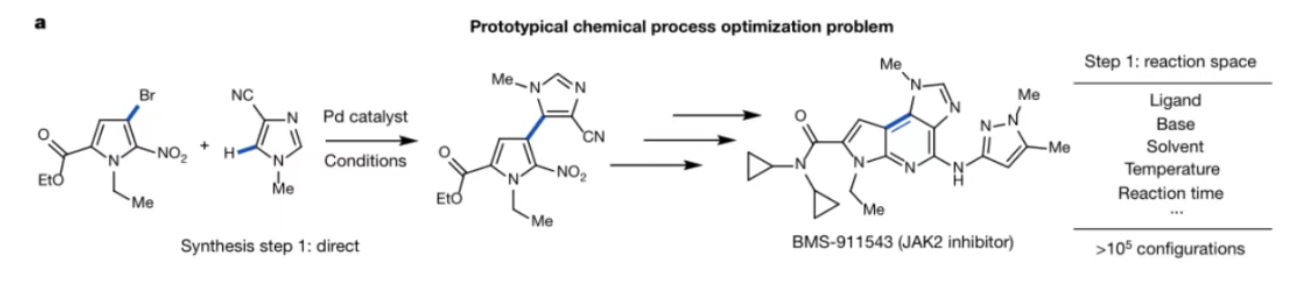
钯催化咪唑直接芳基化反应(药物合成关键步骤)
基于历史研究的变量重要性分析,该反应确定了5个关键优化维度:12种配体、4种碱、4种溶剂、3个温度梯度和 3个浓度梯度 。如果采用传统的全因子实验,将产生高达 12*4*4*3*3=1728种配置可能,这在实际研发中是难以承受的工作量 。
2.2 EDBO的优化路径与成果
MaXFlow引入加入了贝叶斯优化算法的DOE(即 EDBO)。
高效寻优:通过仅3轮(15次)的实验迭代,系统就成功找到了符合目标设定的配方组合 。
卓越结果:在极少的实验次数下,推荐的条件(如使用 KOPiv 作为碱,CgMe-PPh 作为配体,DMAc 为溶剂,浓度 0.153,温度 105℃)实现了98.49%的超高产率,该产率在所有可能的实验结果中高居第6位 。
结论:在处理高维反应空间时,EDBO 的寻优效率与结果质量均呈现出对全因子实验和传统 DOE 的碾压性优势 。
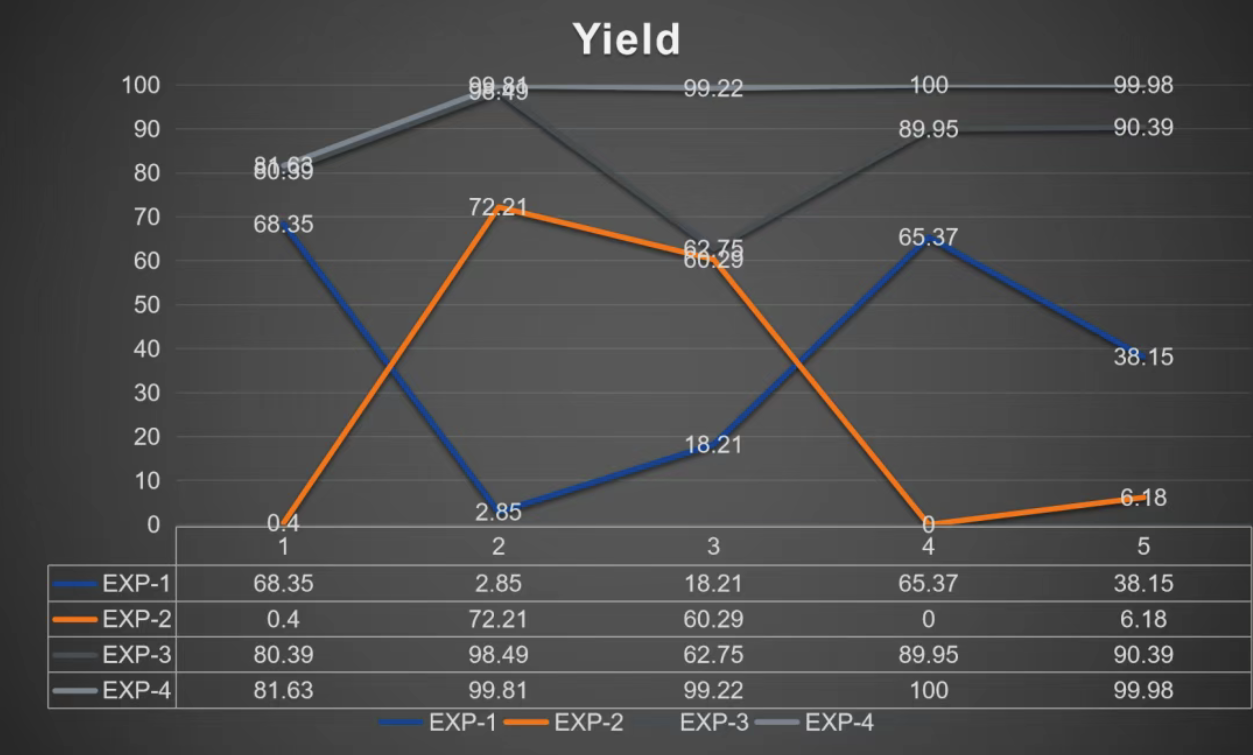
EDBO数据分析工具:
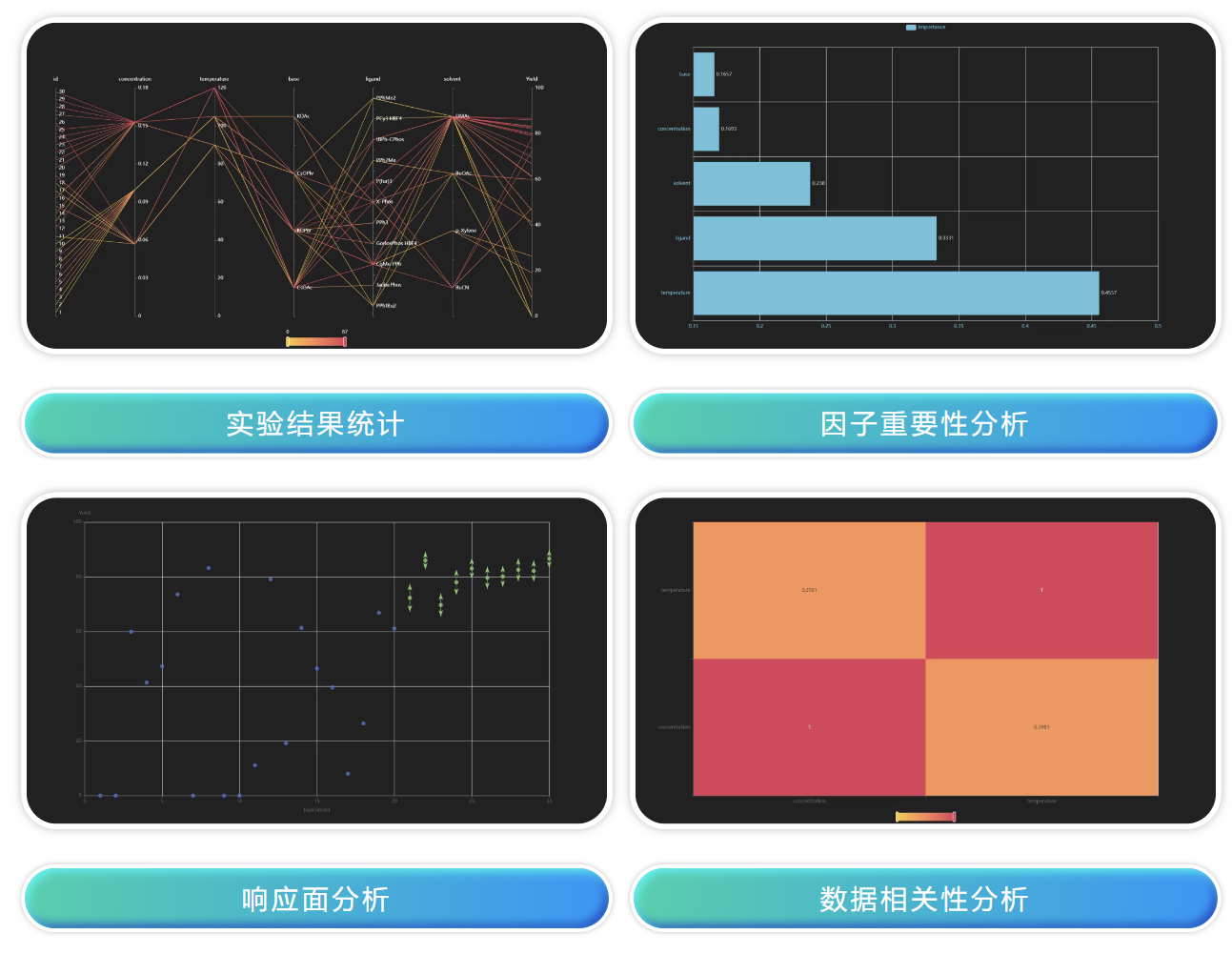
3. 核心应用场景二:大分子单抗多目标制剂优化
MaXFlow 逆向AI实验设计智能体加速CMC工艺与配方设计优化
生物制剂(如单克隆抗体)的配方开发极具挑战性,需要同时兼顾多种生物物理性质并满足严格的工艺约束 。

3.1 复杂的多变量与多目标体系
以单克隆抗体 bococizumab-IgG1为模型,其制剂开发需要调节张力(如氯化钠)、调节渗透压/冻干保护(如蔗糖、海藻糖、山梨醇等)、设置缓冲液(如组氨酸、柠檬酸等,pH 范围 4.8-8.0)以及添加表面活性剂 。 在此案例中,输入变量包含6个可调节参数:山梨醇浓度(0-550 mM)、精氨酸浓度(0-250 mM)、pH(4.5-7.5),以及天冬氨酸 / 谷氨酸 / 乙酸 / HCl 的相对比例(0-1)。同时,必须满足“酸分数总和≤1”的实用制剂约束条件 。
优化的核心目标涉及三大关键生物物理性质 :
1. Tm(熔化温度):反映热稳定性(通过 NANODSF 测定) 。
2. kD(扩散相互作用参数):反映胶体稳定性(通过 DLS 测定) 。
3. RMAgi(气-水界面稳定性):即搅拌应力后保留的单体分数 (通过吸光度法测定)。
3.2 传统 DOE 与 贝叶斯优化的效能对比
在相同的约束条件下,基于贝叶斯优化的平台展现出了惊人的效率:
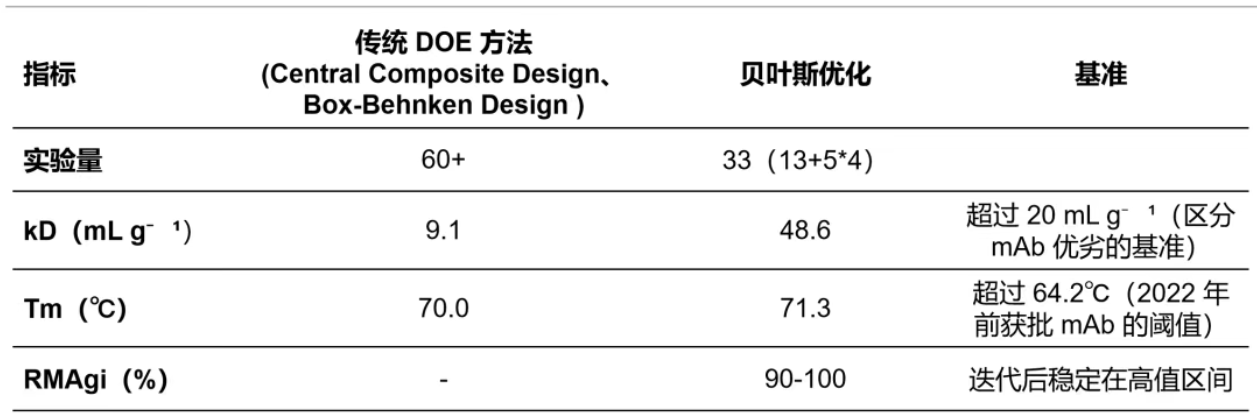
3.3 核心技术优势总结
在生物制剂的多目标优化中,贝叶斯优化的核心优势可以归结为三点 :
1. 极致的实验效率:仅需33次实验即可识别出近帕累托最优制剂,实验量不足传统DOE方法的一半,彻底打破了研发周期瓶颈 。
2. 全局多目标优化策略:采用基于Pareto前沿的EHVI(预期超体积改进)策略,有效避免搜索过早陷入局部区域;同时结合非线性模型,精准刻画辅料对生物物理性质的影响以及它们之间的复杂耦合关系。
3. 高维约束的强兼容性:能够完美整合渗透压、pH等多种工业化生产约束条件,有效克服了传统DOE难以系统处理多约束高阶复杂性的技术盲区,为工程化抗体等难开发生物制剂提供了极其高效的解决方案 。